Fusion nucléaire / Fission Nucléaire
Fission nucléaire :
La fission nucléaire consiste à bombarder des atomes lourds (généralement de l’uranium ou du plutonium) avec des neutrons rapides. Ce bombardement neutronique entraîne la fission du noyau de l’atome, qui produit :
- Des nucléides plus légers
- Une quantité importante d’énergie
- Des neutrons
La fission se réalise sous des conditions de température et de pression normales. La fission nucléaire est une réaction en chaîne exponentielle : les neutrons libérés par la fission d’un noyau iront percuter d’autres noyaux d’atomes. C’est ce qui rend la fission dangereuse : si on ne la contrôle plus, elle ne s’arrête pas.
La fission, comme la fusion sont des réactions naturelles, cependant, la fission est extrêmement rare, alors que la fusion a lieu depuis toujours au cœur des étoiles.
Fusion nucléaire :
La fusion nucléaire consiste à faire se « rassembler » les noyaux de deux atomes, le deutérium et le tritium. Ces deux atomes sont des isotopes lourds de l’hydrogène. Un isotope d’un atome a un nombre de neutrons dans le noyau différent de l’atome original.
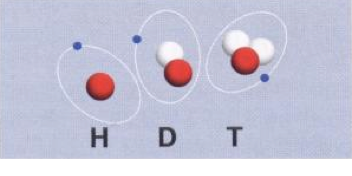
En l’occurrence, l’hydrogène possède 1 proton dans son noyau, le Deutérium possède un proton et un neutron, et enfin le Tritium possède un proton et deux neutrons :
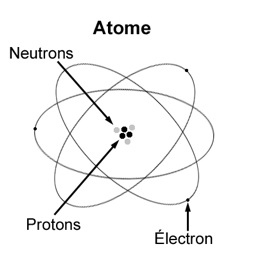
Rappel : Un atome est constitué :
- d’un noyau contenant des protons et des neutrons
- d’un nuage d’électrons
Schéma :
Point plus précis sur les différences entre les trois isotopes :
Ces isotopes sont tous connus sous le nom général d’ « hydrogène ».
Protium (il est appelé communément hydrogène) : Symbole : H
C’est l’isotope le plus répandu, il représente l’élément le plus abondant dans l’univers, mais aussi le plus simple des atomes.
Il n’est pas radioactif, sous des conditions de pression et de température normales, il est à l’état gazeux.
Il devient liquide en dessous d’une température de 20,28°K (soit -252,87°C), et solidifie à 14,01°K (soit -259,14°C).
Deutérium : Symbole : 2H ou D
Il est deux fois plus lourd que le Protium. On estime que, dans la nature, le Deutérium représente 0.015% de la quantité totale d’hydrogène.
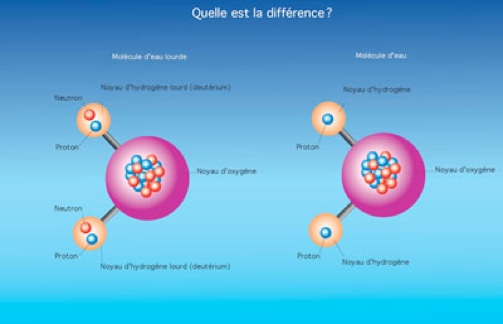
On estime aussi qu’une molécule d’eau sur 7000 est une molécule d’ « eau lourde », autrement appelé oxyde de Deutérium.
C’est une molécule d’eau comprenant, à la place des atomes de Protium, des atomes de Deutérium.
Molécule d’eau lourde et d’eau :
Tritium : Symbole 3H ou T
Il est trois fois plus lourd que le Protium et, contrairement au Deutérium et au Protium, il est radioactif, il émet des rayons β-.
Sa demi-vie est de 12,32 ans.
Note : la demi-vie d’un élément radioactif correspond au temps qu’il met pour perdre la moitié de sa radioactivité. En moyenne, un élément radioactif a besoin de 8 demi-vies pour perdre totalement sa radioactivité. Une demi-vie peut durer de quelques nanosecondes à plusieurs millions d’années.
La radioactivité émise par le Tritium n’est pas très puissante, elle ne peut passer la l’épaisseur de peaux mortes à la surface du corps humain. Le Tritium n’est donc pas dangereux à distance, mais il l’est si des particules de Tritium sont inhalées ou ingérées.
Le Tritium n’est pas présent à l’état naturel, à part quelques quantités infimes dans les hautes couches de l’atmosphère.
Il est produit dans les centrales nucléaires à fission, il représente environ 0,01% des produits de fission.
Le Tritium est donc présent dans le commerce au prix de 100€ le gramme.
La fusion se réalise sous des conditions de pression normale, mais à une température de plusieurs centaines de millions de degrés Celsius.
La fusion à lieu, à la base, au cœur des étoiles.
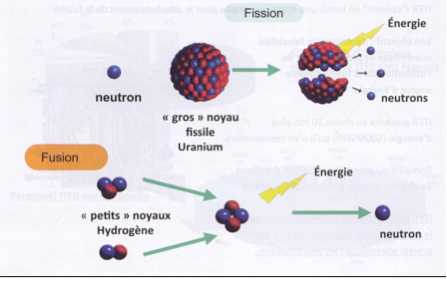
Schéma résumé :
I. - Aspects technologique et historique du projet
II. - Avantages et Inconvenients